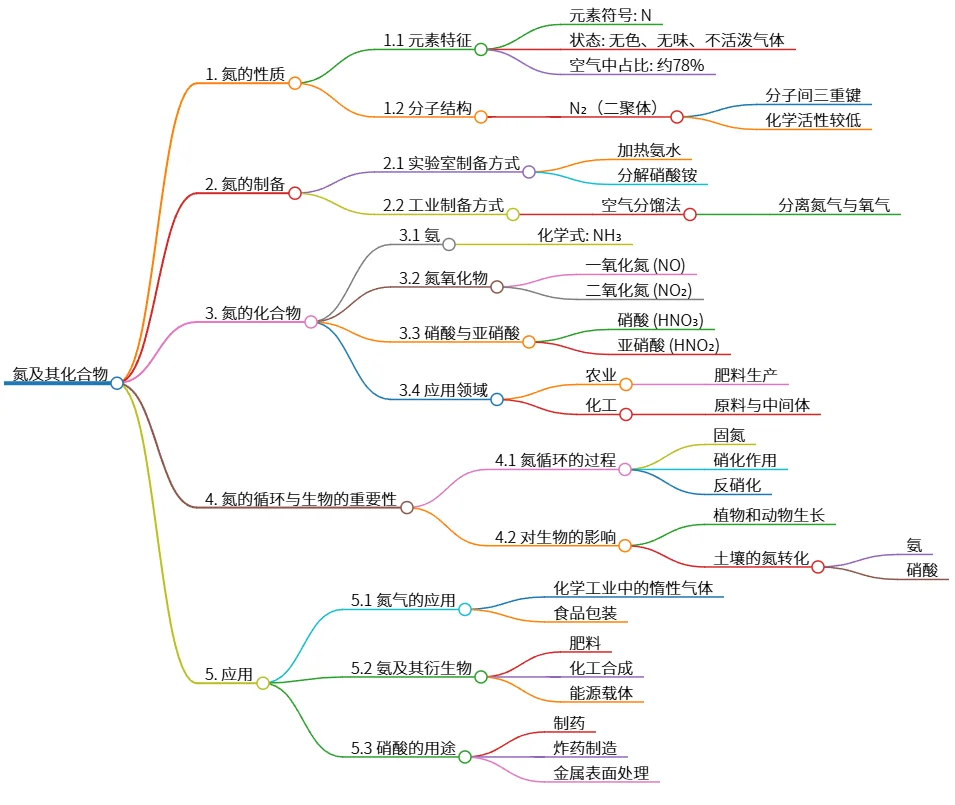
氮及其化合物的性质、制备、应用与生物重要性
该思维导图概述了氮及其化合物的性质、制备、应用及生物重要性。氮是无色无味的气体,主要通过空气分馏法和实验室加热制备。氮的化合物包括氨、氮氧化物及硝酸,广泛应用于农业和化工中。氮循环对于植物和动物的生长至关重要,土壤中的氮可转化为氨和硝酸。应用方面,氮气作为惰性气体在化学工业中使用,氨和硝酸在肥料和药物制造中发挥重要作用。
源码
# 氮及其化合物
## 1. 氮的性质
### 1.1 元素特征
- 元素符号: N
- 状态: 无色、无味、不活泼气体
- 空气中占比: 约78%
### 1.2 分子结构
- N₂(二聚体)
- 分子间三重键
- 化学活性较低
## 2. 氮的制备
### 2.1 实验室制备方式
- 加热氨水
- 分解硝酸铵
### 2.2 工业制备方式
- 空气分馏法
- 分离氮气与氧气
## 3. 氮的化合物
### 3.1 氨
- 化学式: NH₃
### 3.2 氮氧化物
- 一氧化氮 (NO)
- 二氧化氮 (NO₂)
### 3.3 硝酸与亚硝酸
- 硝酸 (HNO₃)
- 亚硝酸 (HNO₂)
### 3.4 应用领域
- 农业
- 肥料生产
- 化工
- 原料与中间体
## 4. 氮的循环与生物的重要性
### 4.1 氮循环的过程
- 固氮
- 硝化作用
- 反硝化
### 4.2 对生物的影响
- 植物和动物生长
- 土壤的氮转化
- 氨
- 硝酸
## 5. 应用
### 5.1 氮气的应用
- 化学工业中的惰性气体
- 食品包装
### 5.2 氨及其衍生物
- 肥料
- 化工合成
- 能源载体
### 5.3 硝酸的用途
- 制药
- 炸药制造
- 金属表面处理
图片